服务介绍:
肿瘤动物模型是肿瘤病因学、发病机制以及防治等研究的重要工具。鼠源细胞接种到小鼠体内,并以此为模型进行疾病发生机制和药物筛选的研究。目前肿瘤化疗所应用的大多数药物,都经动物移植性肿瘤试验而被发现,此模型是筛选抗肿瘤新药中常用的模型,主要适用于免疫调节类药物。
实验结果展示:
1、小鼠荷瘤图

2、小鼠剥瘤图

3、肿瘤生长曲线
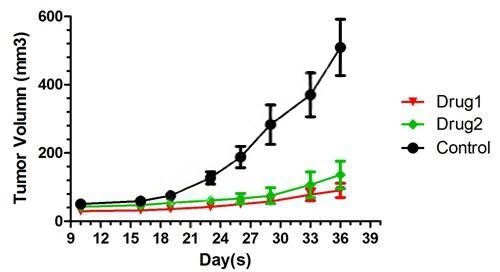
4、组间肿瘤重量对比
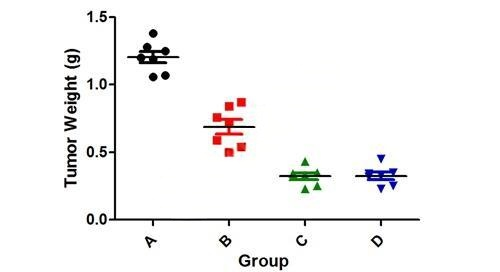
实验流程:
接收方案报价-预付款收取-细胞培养-动物订购-皮下移植瘤接种-成瘤指标监测-药物干预-拍照取材-结果发送
送样运输要求:
冻存细胞需要直接寄到平台,尽量避免因温度转换导致细胞出问题
药品寄送要明确运输条件,储存温度,是否需要避光
寄送细胞和药品时间:周天-周三,特殊情况需和平台沟通确定,避免出现因未及时收货导致样品出现问题
寄送细胞和样品需要附送送样单(备注清楚细胞名称,培养条件等)



