服务介绍:
小鼠血液肺转移瘤又称小鼠肺转移瘤,是一种通过血行散播在肺部形成转移灶的疾病模型。人类肿瘤从生长到转移一般过程是:肿瘤细胞侵袭周围的正常组织和血管,继之癌细胞进入血液循环转运至靶器官,粘附于血管壁上并穿过血管,癌细胞增殖成集落,最后形成转移瘤。采用培养细胞制成的单细胞悬液尾静脉注射接种,则属于人工肺转移,也可在肺部形成肿瘤集落,它可用于肿瘤转移机制的探讨和抗肿瘤生长和转移药物的筛选和研究,和小鼠皮下瘤模型一样,小鼠有正常的免疫系统,人源的肿瘤细胞在小鼠体内难以生长,所以本模型只适用于使用鼠源的肿瘤细胞,同样小鼠的肺转移实验中,也可以通过活体成像来辅助观测肿瘤的生长状况。
名称 | 规格 | 价格(元) |
小鼠肺转移瘤 | 只 | 600起 |
实验结果展示:
1、小鼠肺转移瘤荷瘤图
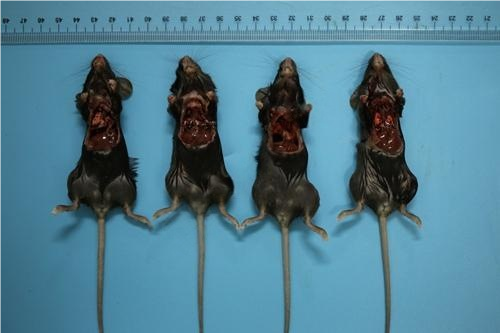
2、肺脏拍照

实验流程:
接收方案报价-预付款收取-细胞培养-动物订购-尾静脉接种细胞-成瘤指标监测 -拍照取材-结果发送
送样运输要求:
冻存细胞需要直接寄到平台,尽量避免因温度转换导致细胞出问题
药品寄送要明确运输条件,储存温度,是否需要避光
寄送细胞和药品时间:周天-周三,特殊情况需和平台沟通确定,避免出现因未及时收货导致样品出现问题