自噬(Autophagy)是真核细胞中高度保守的溶酶体依赖性降解途径,核心作用是维持细胞稳态、应对代谢应激、清除损伤细胞器,也是肿瘤、神经退行性疾病等研究的重要靶点。简单来说,自噬过程中会形成双层膜的自噬体,包裹受损线粒体、错误折叠蛋白等,再与溶酶体融合降解,实现物质循环利用;营养缺乏、氧化应激等刺激会显著诱导自噬活性。而我们用到的MDC(单丹磺酰尸胺),是一种嗜酸性荧光染料,能特异性标记细胞内的酸性囊泡(最典型的就是自噬体)。因自噬体内部呈酸性(pH 4.5-5.5),弱碱性的MDC可进入并结合,在激发波长335-380 nm、发射波长500-540 nm下发出绿色荧光,且荧光强度与自噬体数量正相关——通过荧光显微镜观察或流式细胞仪定量,就能快速评估细胞自噬水平。重点提醒:MDC法仅适用于培养的活细胞/组织,不能用于冻存、固定的细胞、组织及切片染色! |
提前备好以下仪器和试剂,避免实验中途手忙脚乱,所有试剂建议提前检查有效期~• 仪器:荧光显微镜/共聚焦显微镜、CO₂细胞培养箱、超净工作台、倒置显微镜、离心机、移液器、细胞培养板• 试剂:基础培养基、胎牛血清(FBS)、胰蛋白酶-EDTA、MDC试剂取对数生长期细胞,消化计数后,接种于含细胞爬片的24孔板,放入CO₂培养箱中培养24 h,确保细胞贴壁(细胞状态越好,实验结果越准确)。• 模型组:用PBS处理2 h(可根据自身实验需求调整干预条件)将MDC(1000×)原液,按1:1000的比例用Assay Buffer稀释为MDC(1×),即我们后续要用的「MDC染色液」,配制后避光保存。- 吸去培养板中的培养基,用PBS轻轻清洗细胞1-2次,彻底去除残留血清和药物(避免干扰染色)。
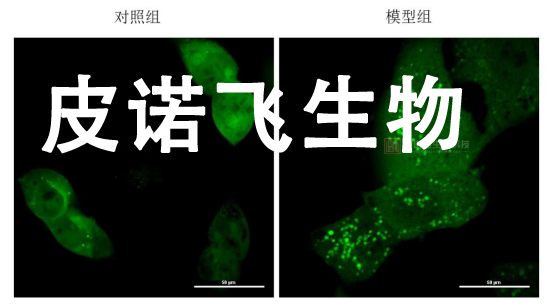
2. 每孔加入1 mL MDC染色工作液,放入细胞培养箱,37℃避光孵育30 min(可根据染色效果,在10-60 min内适当调整孵育时间)。3. 孵育结束后,吸去MDC染色液,用PBS轻轻清洗细胞2-3次,最后每孔加入2 mL PBS,准备观察。在荧光显微镜下观察细胞,找到发出绿色荧光的亮点(即自噬体),拍照记录实验结果即可。以SUM-159PT细胞为例:经PBS处理2 h后,MDC染色可在荧光显微镜下观察到明显的绿色荧光亮点,这就是细胞发生自噬的特征性变化,可根据荧光强度和亮点数量,初步判断自噬水平。
五、注意事项(必看!避免实验失败)
MDC染料对光照极度敏感,从染液配制、染色孵育到观察拍照,全程必须严格避光,否则会导致荧光淬灭,影响实验结果。染色结果受细胞密度、融合度和活性影响极大:所有实验组需保持一致的铺板密度;尽量在细胞对数生长期进行检测;死细胞会产生非特异性背景信号,需提前排除。MDC最佳孵育时间因细胞类型不同而有差异,建议提前做预实验,选择“荧光信号最强、背景最低”的时间点;孵育过长会导致染料在非酸性囊泡蓄积,增加背景干扰。①洗涤时动作要轻,沿孔壁缓慢加液、吸液,避免冲击细胞层导致细胞脱落;②洗涤要充分,未结合的MDC会产生背景荧光,影响定量准确性。再次强调:MDC法只能用于培养的活细胞/组织检测,不能用于冻存、固定的细胞、组织及切片,否则无法获得有效结果。以上就是MDC法检测细胞自噬的完整教程啦,收藏起来,下次做实验直接对照操作~若有实验细节疑问,可在评论区留言交流哦!

